Автор: Денис Аветисян
Обзор посвящен развитию методов компенсации деформаций мозга во время нейрохирургических операций, основанных на анализе данных и машинном обучении.
Пока крипто-инвесторы ловят иксы и ликвидации, мы тут скучно изучаем отчетность и ждем дивиденды. Если тебе близка эта скука, добро пожаловать.
Купить акции "голубых фишек"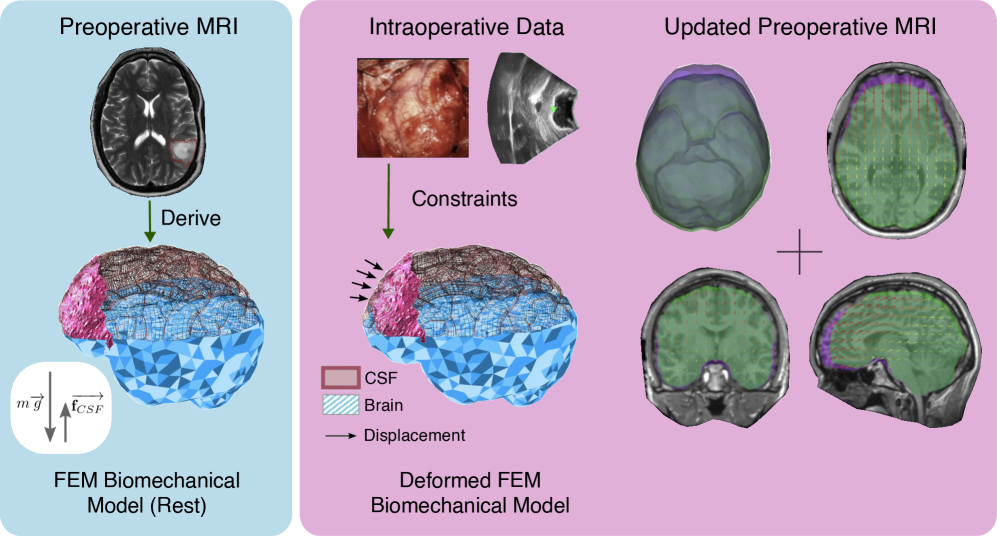
Систематический обзор современных подходов к моделированию деформаций мозга для навигационной нейрохирургии, включая методы глубокого обучения, биомеханическое моделирование и оценку неопределенности.
Несмотря на значительный прогресс в нейрохирургии, точная компенсация деформации мозга, возникающей во время операции, остается сложной задачей. Данный систематический обзор, посвященный моделированию деформации мозга на основе данных для навигационной нейрохирургии (‘A Systematic Review on Data-Driven Brain Deformation Modeling for Image-Guided Neurosurgery’), обобщает современные подходы, основанные на искусственном интеллекте, включая методы глубокого обучения и биомеханическое моделирование. Анализ 41 исследования показал, что, хотя эти модели демонстрируют многообещающую производительность, их клиническое внедрение ограничено проблемами обобщения, стандартизации оценки и учета неопределенности. Каковы перспективы создания надежных и клинически обоснованных решений для компенсации деформации мозга, способных повысить точность и безопасность нейрохирургических вмешательств?
Нейрохирургическая точность: вызовы и решения
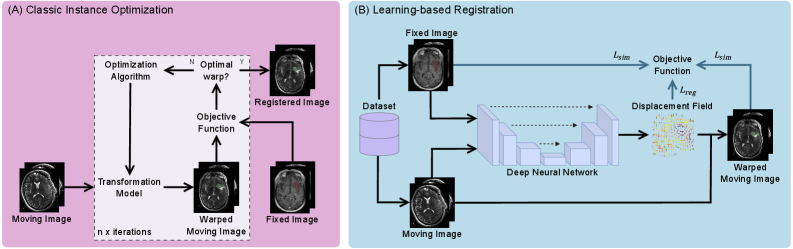
Высокоточная регистрация изображений играет ключевую роль в современной нейрохирургии, обеспечивая возможность навигации хирургических инструментов с беспрецедентной точностью. Эта процедура позволяет хирургам визуализировать критически важные анатомические структуры и безопасно достигать целевых областей мозга, сводя к минимуму повреждение окружающих тканей. Точность выравнивания изображений напрямую влияет на успех операции, уменьшая риск осложнений и способствуя более быстрому восстановлению пациента. В частности, использование передовых методов регистрации позволяет учитывать деформации тканей, возникающие во время операции, и корректировать траекторию инструментов в режиме реального времени, что особенно важно при удалении опухолей или выполнении других сложных процедур.
Традиционные итеративные методы регистрации изображений, несмотря на свою высокую точность, предъявляют значительные требования к вычислительным ресурсам. Этот факт становится критичным в нейрохирургической практике, где требуется оперативное сопоставление предоперационных данных с анатомией пациента в реальном времени. Сложность заключается в том, что каждый шаг итеративного процесса требует существенных затрат времени, что делает невозможным применение этих методов в ситуациях, требующих мгновенной реакции и коррекции во время операции. Более того, растущий объем получаемых данных от интраоперационных методов визуализации лишь усугубляет проблему, приводя к дальнейшему увеличению времени обработки и снижению эффективности хирургического вмешательства. Поэтому разработка альтернативных, более быстрых и эффективных алгоритмов регистрации является ключевой задачей для повышения безопасности и точности нейрохирургических операций.
Внедрение интраоперационной визуализации, такой как КТ и МРТ непосредственно во время хирургического вмешательства, кардинально изменило подходы к нейрохирургии, однако создало и новые сложности. Анатомия мозга подвержена динамическим изменениям в реальном времени — смещению тканей из-за удаления опухоли, изменения давления спинномозговой жидкости или даже физиологической пульсации. Это требует от систем регистрации изображений не только высокой точности, но и способности мгновенно адаптироваться к этим изменениям. Разработка быстрых и устойчивых алгоритмов регистрации, способных компенсировать деформации тканей в режиме реального времени, стала ключевой задачей для обеспечения максимальной безопасности пациента и эффективности операции. Такие технологии позволяют хирургу точно ориентироваться в изменяющейся анатомии, минимизируя риск повреждения здоровых тканей и повышая вероятность полного удаления патологического очага.
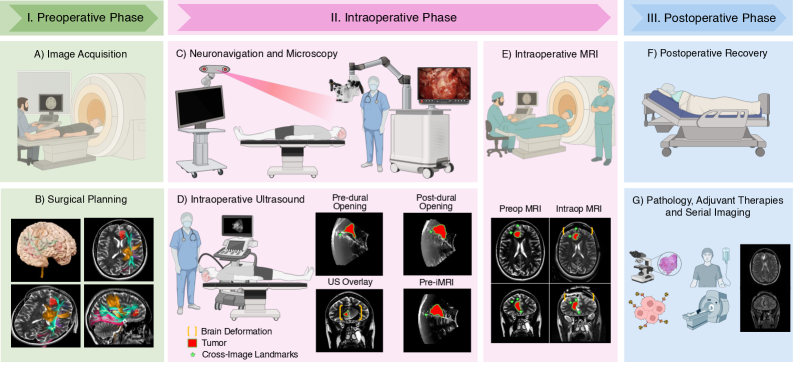
Глубокое обучение на службе точности: автоматизированные пути регистрации
Автоматическая регистрация изображений, осуществляемая посредством DeepLearningRegistration, представляет собой перспективное решение для повышения скорости и эффективности процесса выравнивания медицинских изображений. Традиционные методы, требующие значительных вычислительных ресурсов и ручной настройки параметров, заменяются нейронными сетями, способными к параллельной обработке данных и обучению на больших наборах данных. Это позволяет существенно сократить время, необходимое для выравнивания изображений, и повысить точность, особенно в случаях сложных деформаций тканей. Использование нейронных сетей также позволяет снизить зависимость от экспертных знаний и автоматизировать рутинные задачи, что является критически важным для клинической практики и научных исследований.
Архитектуры свёрточных нейронных сетей (CNN) и графовых нейронных сетей (GNN) демонстрируют высокую эффективность в задачах обработки медицинских изображений, в частности, при регистрации тканей мозга. CNN способны автоматически извлекать иерархические признаки из изображений, выявляя закономерности, связанные с анатомическими структурами и деформациями. GNN, в свою очередь, эффективно моделируют сложные взаимосвязи между точками данных, что позволяет точно описывать нелинейные деформации тканей мозга. Комбинирование этих архитектур позволяет создавать модели, способные одновременно извлекать признаки и учитывать топологические свойства тканей, повышая точность и надёжность процесса регистрации.
PointNet представляет собой нейронную сеть, разработанную для непосредственной обработки данных в виде 3D облаков точек, что позволяет обходить необходимость предварительной обработки, такой как вокселизация или преобразование в меш-представление. Этот подход обеспечивает эффективное извлечение признаков непосредственно из необработанных 3D-данных, сохраняя при этом информацию о геометрии и топологии. В контексте анализа анатомических структур, PointNet позволяет точно представлять и анализировать сложные формы, такие как органы и ткани, без потери детализации, что критически важно для задач регистрации изображений и сегментации. Архитектура PointNet использует симметричные функции для обеспечения инвариантности к перестановкам точек в облаке, что обеспечивает надежность и стабильность результатов анализа.
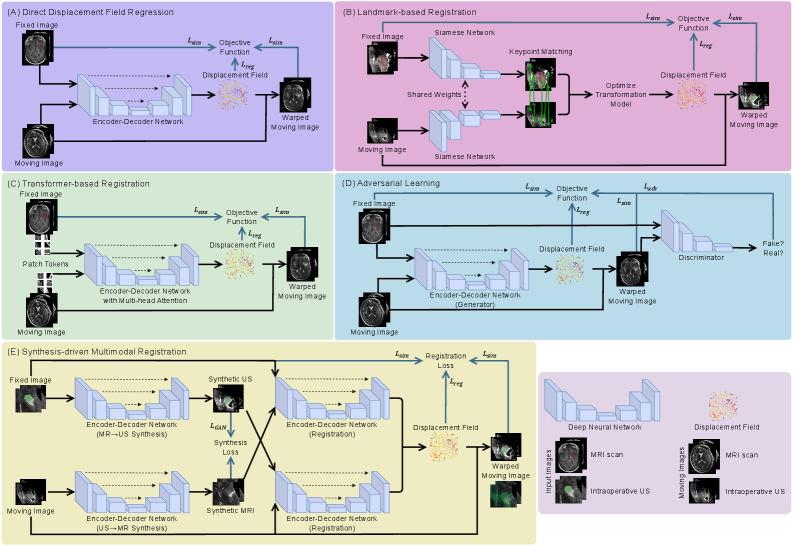
За пределами выравнивания: количественная оценка неопределенности регистрации
Оценка неопределенности (Uncertainty Estimation) представляет собой критически важный этап в регистрации медицинских изображений, обеспечивающий количественную оценку надежности полученных результатов. Эта методика позволяет выявлять потенциальные неточности в деформации и позиционировании изображений, что особенно важно в нейрохирургии. Предоставляя информацию о степени достоверности регистрации, система оповещает хирурга о областях, где требуется повышенное внимание или дополнительная проверка, снижая риски, связанные с неточным наведением инструментов во время операции. Количественная оценка неопределенности позволяет врачу принимать обоснованные решения, основанные не только на зарегистрированном изображении, но и на оценке ее надежности.
Для обучения и валидации алгоритмов деформационной регистрации на основе глубокого обучения критически важны крупномасштабные наборы данных, такие как BraTS и ReMIND. Эти базы данных предоставляют достаточное количество изображений мозга с различными патологиями и анатомическими особенностями, что позволяет моделям глубокого обучения обобщать и эффективно компенсировать деформации. Использование этих данных позволяет оценивать надежность и точность алгоритмов в различных клинических сценариях и обеспечивает возможность их валидации на независимых наборах изображений, что необходимо для обеспечения безопасности и эффективности в клинической практике.
Систематический обзор 4141 исследования продемонстрировал значительный рост применения методов глубокого обучения для компенсации деформации мозга в нейрохирургии, осуществляемой под контролем изображений. В настоящее время около 75% всех исследуемых работ используют подходы, основанные на глубоком обучении, что свидетельствует о преобладании этих технологий в данной области и их активном внедрении в научные исследования.
Проведенная валидация на масштабных наборах данных, таких как BraTS и ReMIND, демонстрирует потенциал методов глубокого обучения для достижения передовых результатов в области регистрации медицинских изображений. Зафиксированное время обновления составляет менее 60 секунд, что соответствует требованиям к скорости обработки в клинической практике. При этом, достигнутая целевая точность составляет менее 3 мм, что является критически важным параметром для обеспечения безопасности и эффективности хирургических вмешательств, осуществляемых с применением навигационных систем на основе зарегистрированных изображений.
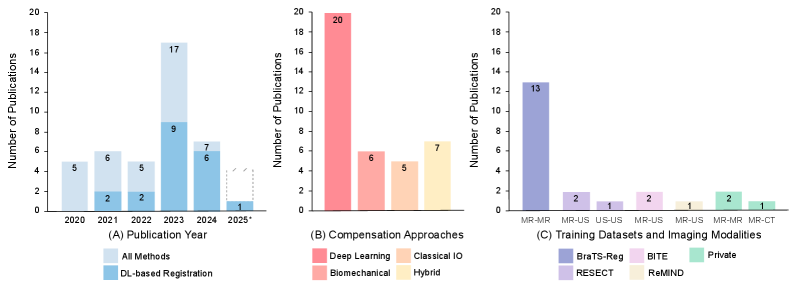
Моделирование динамики мозга: биомеханическая интеграция
Биомеханическое моделирование представляет собой передовой подход к симуляции деформации мозговой ткани, учитывающий её физические свойства и влияние хирургических факторов. Данная методика позволяет значительно повысить точность и реалистичность процессов регистрации медицинских изображений, что особенно важно при планировании нейрохирургических вмешательств. Вместо упрощенных геометрических преобразований, биомеханическая модель рассчитывает, как ткань мозга деформируется под воздействием инструментов, удаления опухоли или других хирургических манипуляций. Такой подход позволяет создать более достоверное представление о взаимном расположении структур мозга во время операции, что, в свою очередь, способствует более точному нацеливанию и снижению рисков для пациента. Точность моделирования напрямую зависит от корректного определения физических характеристик ткани, таких как модуль упругости и коэффициент Пуассона, а также от учета индивидуальных особенностей каждого пациента.
Метод нейронных сетей, основанных на физических принципах (PINNs), представляет собой инновационный подход к моделированию деформации тканей мозга. В отличие от традиционных методов глубокого обучения, PINNs интегрируют непосредственно физические законы, описывающие поведение ткани, в процесс обучения нейронной сети. Это осуществляется посредством использования специальных функций потерь — PhysicsInformedLoss functions — которые штрафуют отклонения от физически обоснованных решений. По сути, сеть обучается не только соответствовать данным изображения, но и соблюдать известные физические ограничения, что значительно повышает точность и реалистичность моделирования деформаций, возникающих во время нейрохирургических вмешательств. \nabla \cdot \sigma + f = 0 — типичное уравнение, которое может быть включено в функцию потерь для обеспечения соответствия модели законам механики сплошных сред.
Гибридные методы регистрации, объединяющие сильные стороны глубокого обучения и итеративной оптимизации, представляют собой перспективный подход к повышению надежности и эффективности нейрохирургической навигации. В отличие от традиционных методов, полагающихся исключительно на итеративные алгоритмы, или же полностью на нейронные сети, гибридные системы используют глубокое обучение для предварительной оценки деформации тканей мозга и установления грубого соответствия между предоперационными изображениями и данными, полученными во время операции. Затем, итеративные алгоритмы оптимизации используются для уточнения этого соответствия, минимизируя разницу между моделями и реальными анатомическими ориентирами. Такой симбиоз позволяет преодолеть ограничения каждого подхода по отдельности: глубокое обучение обеспечивает скорость и способность к обобщению, в то время как итеративная оптимизация гарантирует точность и устойчивость к шумам и артефактам. В результате, гибридные методы регистрации открывают возможности для более точного планирования операций, уменьшения риска повреждения здоровых тканей и улучшения исходов для пациентов.
Исследование, посвященное моделированию деформации мозга в нейрохирургии, демонстрирует, что даже самые передовые вычислительные методы не избавлены от систематических ошибок. Подобно тому, как человеческий разум склонен к когнитивным искажениям, моделирование деформации мозга, несмотря на использование глубокого обучения и биомеханических моделей, требует тщательной валидации и оценки неопределенности. Томас Гоббс заметил: «Люди руководствуются не разумом, а страхом и надеждой». Эта фраза находит отклик в представленной работе, ведь стремление к точному моделированию деформации мозга продиктовано желанием минимизировать риски для пациента, а не только стремлением к теоретической совершенству. Понимание этих человеческих факторов, влияющих на создание и интерпретацию моделей, критически важно для улучшения клинических результатов.
Куда же мы движемся?
Представленные методы моделирования деформации мозга, безусловно, впечатляют своей сложностью. Однако, не стоит забывать, что каждая модель — это лишь упрощение, попытка вместить хаотичную биологическую реальность в рамки математических формул. И эта реальность неизменно вносит свои поправки. Оптимизация алгоритмов глубокого обучения и интеграция биомеханических моделей — это, конечно, важные шаги, но они не решают фундаментальной проблемы: мозг — не статичный объект, а динамическая система, подверженная множеству непредсказуемых факторов.
Особое внимание следует уделить не только точности моделирования, но и оценке неопределённости. Ведь любая стратегия работает, пока в неё не начинают верить слишком сильно. Игнорирование погрешностей и предположений, лежащих в основе этих моделей, может привести к катастрофическим последствиям в клинической практике. Более того, следует признать, что «золотой стандарт» регистрации изображений, на котором порой строятся все эти сложные вычисления, сам по себе далёк от идеала и подвержен субъективным ошибкам.
В перспективе, вероятно, потребуется переход от чисто вычислительных методов к более целостному подходу, учитывающему индивидуальные особенности пациента, его физиологическое состояние и даже психологические факторы. Иначе говоря, нужно научиться видеть не только деформацию мозга, но и человека, который за ней скрывается. И тогда, возможно, мы сможем приблизиться к действительно эффективной и безопасной хирургии.
Оригинал статьи: https://arxiv.org/pdf/2602.10155.pdf
Связаться с автором: https://www.linkedin.com/in/avetisyan/
Смотрите также:
- Обзор Motorola Razr 50 Ultra
- Фотографируем муравьёв с Андреем Павловым
- Nikon D7200
- Преодолевая границы масштабируемости рекомендательных систем
- Warhammer 40,000: Space Marine 2 — Список всех врагов и боссов на данный момент
- Лучшие ноутбуки с матовым экраном. Что купить в мае 2026.
- vivo iQOO Z7 ОБЗОР: тонкий корпус, скоростная зарядка, чёткое изображение
- vivo S50 Pro mini ОБЗОР: чёткое изображение, беспроводная зарядка, скоростная зарядка
- Обзор телеобъектива Nikkor 70-300 VR AF-S
- Обзор Nikon D5500 DX
2026-02-12 13:19
