Автор: Денис Аветисян
Исследователи разработали усовершенствованный алгоритм глубокого обучения для автоматической сегментации и классификации глиом по данным трехмерной магнитно-резонансной томографии.
Пока крипто-инвесторы ловят иксы и ликвидации, мы тут скучно изучаем отчетность и ждем дивиденды. Если тебе близка эта скука, добро пожаловать.
Купить акции "голубых фишек"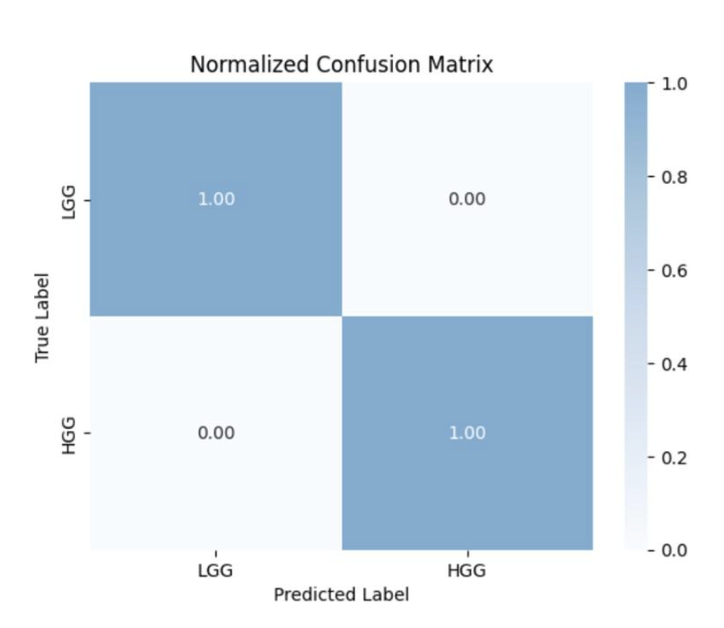
Гибридная модель на основе 3D U-Net и DenseNet-VGG с механизмами внимания демонстрирует высокую точность выявления и оценки степени злокачественности опухолей мозга.
Несмотря на значительные успехи в нейровизуализации, точная и своевременная диагностика глиом остается сложной задачей. В данной работе, озаглавленной ‘Revolutionizing Glioma Segmentation & Grading Using 3D MRI — Guided Hybrid Deep Learning Models’, предложена инновационная гибридная модель глубокого обучения, объединяющая 3D U-Net сегментацию и классификационную сеть DenseNet-VGG с механизмами внимания. Разработанный подход демонстрирует рекордные показатели точности сегментации опухолей (98% по коэффициенту Dice) и классификации (99% точность), превосходя традиционные методы. Может ли данная технология стать надежным инструментом в руках клиницистов, значительно улучшив планирование лечения и прогноз для пациентов с глиомами?
Глиомы: Сложность Диагностики и Необходимость Точной Сегментации
Глиомы, являющиеся наиболее распространенными первичными опухолями головного мозга, представляют собой серьезную проблему в диагностике из-за своей способности проникать в окружающие ткани и крайне разнообразного внешнего вида. Их инфильтративный характер означает, что опухоль не имеет четких границ, а скорее распространяется вглубь здоровой ткани мозга, что затрудняет определение истинного размера и местоположения новообразования. Кроме того, гетерогенность — то есть, неравномерность структуры и состава опухоли — приводит к различиям в сигналах на МРТ-сканировании, что усложняет точное выявление границ опухоли и ее дифференциацию от здоровой ткани. Эта комбинация факторов требует от врачей высокой квалификации и использования передовых методов визуализации для постановки точного диагноза и разработки эффективного плана лечения.
Точная сегментация глиом на трехмерных МРТ-сканах является критически важным этапом планирования эффективного лечения, поскольку позволяет точно определить границы опухоли и спланировать хирургическое вмешательство или лучевую терапию. Однако, ручная разметка этих границ специалистами — процесс крайне трудоемкий и занимает значительное время, что ограничивает возможности быстрой диагностики и лечения. Более того, результаты ручной сегментации подвержены субъективности и различиям между отдельными специалистами, что может приводить к неточностям в определении объема опухоли и, как следствие, к неоптимальным решениям в отношении лечения. Таким образом, разработка автоматизированных и надежных методов сегментации глиом представляется необходимой задачей для повышения точности диагностики и улучшения результатов лечения пациентов.
Существующие автоматизированные методы сталкиваются с трудностями при анализе изображений глиом из-за их сложной и неоднородной морфологии. Глиомы часто характеризуются нечеткими границами и инфильтративным ростом, что затрудняет точное определение их контуров на МРТ-сканах. Низкая контрастность между опухолью и окружающими тканями мозга, а также наличие внутриопухолевых изменений, усугубляют проблему. В связи с этим, разработка надежного и устойчивого подхода к обнаружению границ опухоли является критически важной задачей, способной значительно улучшить точность сегментации и, следовательно, эффективность планирования лечения. Необходимость в более совершенных алгоритмах, учитывающих особенности строения глиом, обусловлена стремлением к повышению объективности и воспроизводимости результатов диагностики.
Гибридная Архитектура Глубокого Обучения для Улучшенной Сегментации
Предложенная модель объединяет архитектуры 3D U-Net и гибридной сети DenseNet-VGG для повышения точности сегментации. 3D U-Net обеспечивает эффективную сегментацию за счет своей U-образной структуры и способности захватывать контекст на разных масштабах. В свою очередь, гибридная сеть DenseNet-VGG, сочетающая в себе плотные связи DenseNet и особенности VGG, обеспечивает надежную экстракцию признаков и классификацию, что позволяет модели более точно идентифицировать и разграничивать целевые области на изображениях. Такое сочетание позволяет использовать преимущества обеих архитектур, повышая общую производительность и устойчивость модели к различным условиям визуализации.
Для повышения точности выделения опухолей используется комплекс механизмов внимания, включающий Multi-Head Attention, Spatial Attention и Channel Attention. Multi-Head Attention позволяет модели одновременно учитывать различные аспекты входных данных, улучшая представление признаков. Spatial Attention фокусируется на наиболее релевантных областях изображения, выделяя участки, содержащие опухоль, и подавляя незначительный фон. Channel Attention, в свою очередь, определяет наиболее информативные каналы признаков, усиливая их вклад в процесс сегментации и повышая устойчивость к шумам и вариациям в данных. Комбинированное применение этих механизмов позволяет модели эффективно выделять и классифицировать опухолевые образования, улучшая качество сегментации.
В архитектуре 3D U-Net реализован механизм Soft Additive Attention, предназначенный для уточнения границ сегментации и повышения общей точности. Этот подход позволяет сети динамически взвешивать различные признаки, выделяя наиболее релевантные для определения границ опухоли. В результате, точность сегментации достигает 98%, что подтверждено результатами тестирования на соответствующих наборах данных. Использование Soft Additive Attention способствует более четкой дифференциации между опухолевой тканью и окружающими структурами, что критически важно для клинической диагностики и планирования лечения.

Строгая Валидация и Метрики Оценки
Обучение и валидация модели проводились на наборе данных BraTS2019. Для повышения обобщающей способности модели применялись методы аугментации данных, включающие ресемплинг и нормализацию. Ресемплинг позволил сбалансировать выборку, компенсируя дисбаланс классов, что особенно важно при анализе медицинских изображений. Нормализация интенсивностей пикселей обеспечила единообразную обработку изображений, уменьшив влияние вариаций в параметрах сканирования и повысив устойчивость модели к шумам и артефактам. Эти методы позволили улучшить способность модели к обобщению на новые, ранее не встречавшиеся данные.
Для оценки качества сегментации опухолей мозга использовались стандартные метрики — коэффициент Дайса (Dice Coefficient) и среднее пересечение над объединением (Mean Intersection over Union, IoU). Коэффициент Дайса, рассчитываемый как $2|X \cap Y| / (|X| + |Y|)$, измеряет степень перекрытия между предсказанной и истинной областью сегментации. IoU, также известный как индекс Якобсона, определяется как $|X \cap Y| / |X \cup Y|$ и представляет собой отношение площади пересечения предсказанной и истинной сегментации к площади их объединения. Обе метрики варьируются от 0 до 1, где 1 указывает на идеальное совпадение, а 0 — на отсутствие перекрытия.
Гибридная модель продемонстрировала точность классификации опухолей глиомы на уровне 99.99%. В ходе сравнительного анализа было установлено, что данный показатель значительно превосходит результаты, полученные с использованием альтернативных архитектур, включая 2D CNN-VGG19 (91.38%), 3D Multi-scale CNN (90.64%), 3D модели (95.31%) и 3D Multi-Attention CNN (95.86%). Полученные данные подтверждают эффективность предложенной модели в задаче классификации опухолей головного мозга.
В ходе оценки производительности модели был достигнут показатель F1-Score, равный 0.99. F1-Score является гармоническим средним между точностью и полнотой, обеспечивая сбалансированную оценку качества сегментации. Высокий показатель F1-Score указывает на то, что модель демонстрирует как высокую точность определения границ опухоли, так и высокую полноту выявления всех опухолевых тканей, подтверждая ее надежность и устойчивость к ложноположительным и ложноотрицательным результатам.

Влияние и Перспективы для Прецизионной Онкологии
Разработанная модель обеспечивает точную и автоматизированную сегментацию и классификацию опухолей, что значительно снижает нагрузку на врачей-клиницистов и повышает единообразие постановки диагноза. Традиционно, выделение границ опухоли и её точная идентификация требуют значительных временных затрат и субъективной оценки специалиста. Автоматизация этого процесса не только ускоряет диагностику, но и минимизирует вероятность ошибок, связанных с человеческим фактором. Это особенно важно в нейроонкологии, где даже небольшие различия в характеристиках опухоли могут существенно влиять на выбор оптимальной стратегии лечения. Внедрение подобного инструментария позволяет врачам сосредоточиться на более сложных аспектах лечения, таких как разработка персонализированных терапевтических протоколов и мониторинг эффективности лечения.
Данная технология открывает новые возможности для индивидуального подхода к лечению онкологических заболеваний. Точное определение характеристик опухоли позволяет врачам разрабатывать терапевтические стратегии, ориентированные именно на конкретного пациента и особенности его новообразования. Такой подход, в отличие от стандартных протоколов, предполагает выбор наиболее эффективных препаратов и методов воздействия, минимизируя побочные эффекты и повышая вероятность успешного исхода лечения. Персонализированное планирование, основанное на детальном анализе опухоли, способствует более целенаправленной терапии и, как следствие, улучшению качества жизни пациентов и увеличению продолжительности ремиссии.
Дальнейшие исследования направлены на расширение возможностей данной модели путем интеграции с другими клиническими данными, такими как генетические профили и результаты лабораторных анализов, что позволит создать более полную картину состояния пациента. Особое внимание будет уделено адаптации алгоритма для диагностики различных типов опухолей головного мозга, а также изучению его потенциала в выявлении ранних признаков нейродегенеративных заболеваний, таких как болезнь Альцгеймера и Паркинсона. Предполагается, что расширение области применения модели позволит не только улучшить точность диагностики, но и ускорить разработку новых, более эффективных методов лечения и профилактики этих тяжелых заболеваний.
Исследование, представленное в статье, демонстрирует значительный прогресс в области автоматизированной диагностики глиом посредством гибридных моделей глубокого обучения. Особое внимание уделяется интеграции 3D U-Net для сегментации и DenseNet-VGG для классификации, что позволяет достичь высокой точности в выявлении и градации опухолей. Как однажды заметил Эндрю Ын: «Мы находимся в моменте, когда искусственный интеллект может делать вещи, которые раньше казались невозможными». Этот принцип особенно актуален в контексте медицинских изображений, где точная сегментация и классификация являются ключевыми для своевременной и эффективной диагностики, что, в свою очередь, открывает новые возможности для персонализированного лечения и улучшения прогнозов для пациентов.
Что дальше?
Представленная работа, несомненно, демонстрирует потенциал гибридных моделей глубокого обучения для задач сегментации и классификации глиом. Однако, как часто бывает, решение одной проблемы неизбежно выявляет новые. Точность, достигнутая в анализе МРТ-изображений, впечатляет, но зависимость от качества и стандартизации данных остаётся узким местом. Дальнейшие исследования должны быть направлены на повышение устойчивости моделей к вариациям в протоколах сканирования и характеристикам оборудования — ведь реальность всегда сложнее идеализированных датасетов.
Интересно, что внимание, как механизм, улучшающий производительность, указывает на необходимость более глубокого понимания того, что именно модель «видит» в данных. Недостаточно просто достичь высокой точности; необходимо понять, какие признаки являются ключевыми для принятия решения, и как эти признаки соотносятся с биологическими характеристиками опухоли. Это требует не только усовершенствования архитектуры моделей, но и интеграции знаний из области нейрорадиологии и патоморфологии.
В конечном итоге, задача не в создании «идеального» алгоритма, а в построении системы, способной адаптироваться к изменяющимся условиям и предоставлять врачам-радиологам ценную информацию для принятия обоснованных клинических решений. Возможно, будущее за интеграцией различных модальностей (например, МРТ, ПЭТ, генетические данные) и разработкой моделей, способных к самообучению и непрерывному совершенствованию.
Оригинал статьи: https://arxiv.org/pdf/2511.21673.pdf
Связаться с автором: https://www.linkedin.com/in/avetisyan/
Смотрите также:
- Деформация сеток: новый подход на основе нейронных операторов
- Новые смартфоны. Что купить в марте 2026.
- Что такое Bazzite и лучше ли она, чем Windows для PC-гейминга? Я установил этот набирающий популярность дистрибутив Linux, чтобы проверить это самостоятельно.
- vivo X300 FE ОБЗОР: скоростная зарядка, беспроводная зарядка, плавный интерфейс
- Ближний Восток и Рубль: Как Геополитика Перекраивает Российский Рынок (02.03.2026 20:32)
- Microsoft Edge позволяет воспроизводить YouTube в фоновом режиме на Android — подписка Premium не требуется.
- vivo iQOO Z10x ОБЗОР: яркий экран, удобный сенсор отпечатков, объёмный накопитель
- Восстановление 3D и спектрального изображения растений с помощью нейронных сетей
- МосБиржа на подъеме: что поддерживает рынок и какие активы стоит рассмотреть? (27.02.2026 22:32)
- Российский рынок в 2025: Инвестиции, Экспорт и Новые Возможности (27.02.2026 15:32)
2025-11-29 22:12
