Автор: Денис Аветисян
Исследователи предлагают инновационную методику, использующую возможности мультимодальной магнитно-резонансной томографии и адаптивной обработки данных для более точного выявления границ опухолей мозга.
Пока крипто-инвесторы ловят иксы и ликвидации, мы тут скучно изучаем отчетность и ждем дивиденды. Если тебе близка эта скука, добро пожаловать.
Купить акции "голубых фишек"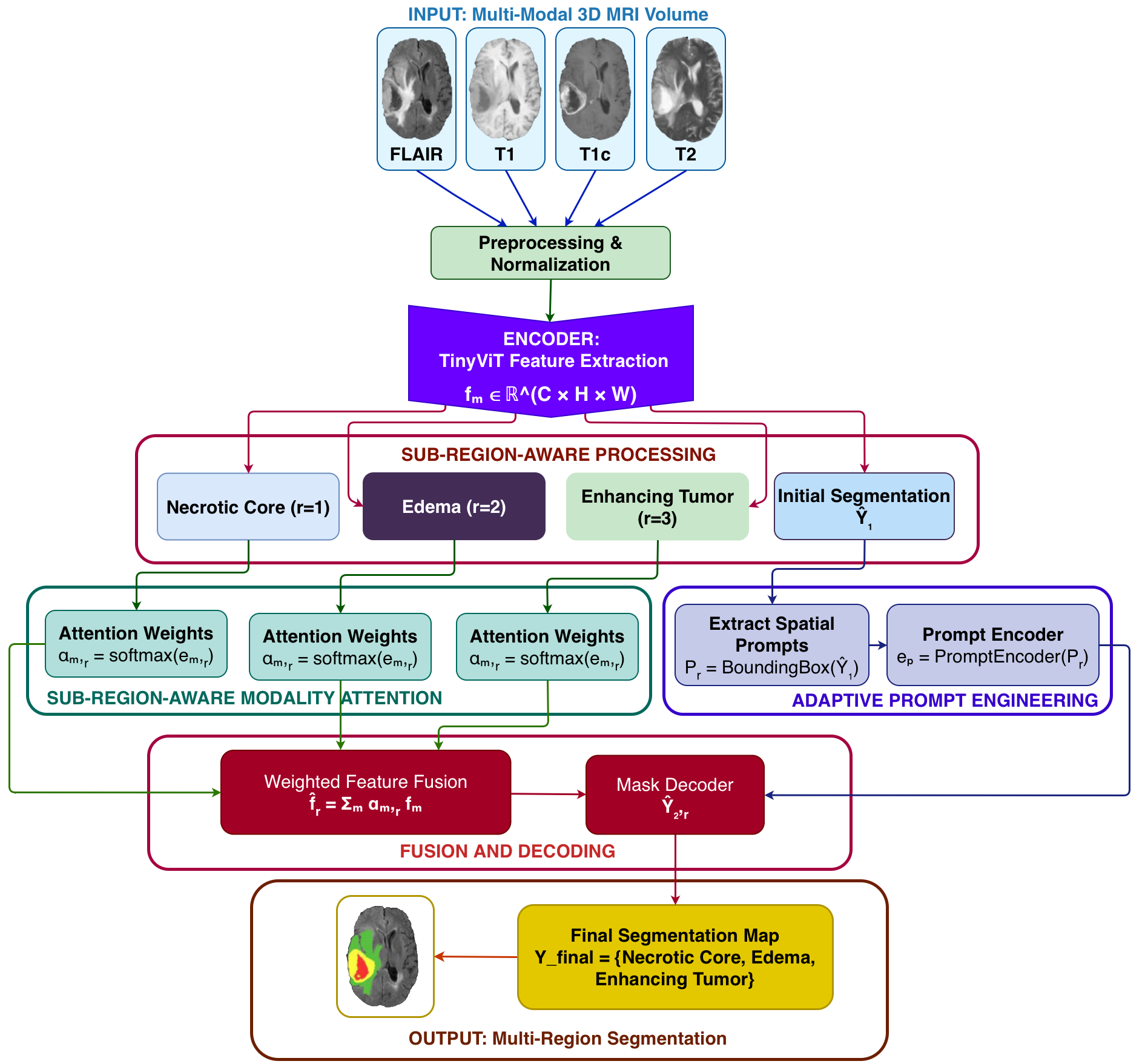
Предлагаемый фреймворк улучшает сегментацию опухолей мозга за счет адаптивного объединения данных разных модальностей МРТ и анализа под-областей опухоли, особенно некротического ядра.
Несмотря на значительный прогресс в области медицинского анализа изображений, адаптация мощных предварительно обученных моделей к мультимодальным данным остается сложной задачей. В данной работе, посвященной теме ‘Sub-Region-Aware Modality Fusion and Adaptive Prompting for Multi-Modal Brain Tumor Segmentation’, предложен новый подход к сегментации опухолей головного мозга, основанный на адаптивном объединении данных различных модальностей МРТ и уточнении прогнозов с учетом особенностей подрегионов опухоли. Предложенная архитектура позволяет добиться существенного повышения точности сегментации, особенно в сложных областях, таких как некротический центр. Способна ли эта методика стать основой для создания более надежных и эффективных систем поддержки принятия решений в нейроонкологии?
Точность в деталях: вызовы сегментации опухолей головного мозга
Точное определение границ опухолей головного мозга имеет решающее значение для разработки эффективных планов лечения и последующего мониторинга состояния пациента. Однако, эта задача представляет собой значительную сложность из-за анатомической изменчивости мозга и вариабельности изображений, получаемых при различных методах визуализации. Различия в структуре мозга у разных людей, а также факторы, влияющие на качество снимков — такие как разрешение, контрастность и наличие артефактов — затрудняют автоматическое или даже ручное выделение опухолевых тканей. Нечеткое определение границ может привести к недооценке или переоценке объема опухоли, что напрямую влияет на выбор оптимальной стратегии лечения и, следовательно, на прогноз для пациента. Поэтому разработка надежных и точных методов сегментации опухолей мозга остается приоритетной задачей в нейрорадиологии и медицинской визуализации.
Традиционные методы сегментации опухолей головного мозга часто сталкиваются с трудностями при точном определении границ новообразований, что приводит к потенциальной недооценке или переоценке их объема. Эта неточность напрямую влияет на планирование лечения и мониторинг состояния пациента. Нечеткое определение границ опухоли может привести к тому, что часть новообразования останется без воздействия, либо, наоборот, затронутся здоровые ткани. В результате, выбор оптимальной стратегии лечения, будь то хирургическое вмешательство, лучевая терапия или химиотерапия, становится затрудненным, а эффективность терапии снижается. Погрешность в оценке объема опухоли также влияет на оценку динамики заболевания и своевременное выявление рецидивов, что критически важно для улучшения прогноза пациентов.
Использование многомодальной визуализации, включающей данные из различных источников, таких как магнитно-резонансная томография (МРТ), компьютерная томография (КТ) и позитронно-эмиссионная томография (ПЭТ), значительно обогащает информацию о новообразованиях головного мозга. Однако, простое объединение этих данных недостаточно. Эффективные стратегии интеграции, позволяющие учесть особенности каждого метода и компенсировать их ограничения, являются ключевыми для точного определения границ опухоли. Различные подходы к слиянию данных, включая методы на основе машинного обучения, позволяют выделить признаки, невидимые при использовании только одного типа визуализации, что, в свою очередь, повышает надежность сегментации и улучшает планирование лечения.
Автоматизированная сегментация опухолей головного мозга представляется перспективным решением для повышения точности и скорости диагностики, однако требует разработки надежных методов, способных адаптироваться к разнообразию медицинских изображений. Особую сложность представляет обработка данных, подобных тем, что содержатся в наборе BraTS 2020, характеризующемся значительными различиями в качестве снимков, анатомических особенностях пациентов и типах опухолей. Эффективные алгоритмы должны демонстрировать устойчивость к этим вариациям, обеспечивая стабильно высокую точность сегментации даже в условиях неоднородных и сложных наборов данных, что критически важно для надежного планирования лечения и мониторинга прогресса заболевания.
Архитектурные решения и стратегии мультимодального слияния
Архитектура U-Net стала основополагающей в области сегментации медицинских изображений, предоставляя мощную структуру для извлечения признаков и выделения контуров. Её ключевым компонентом является энкодер-декодер, который позволяет захватывать как контекстную информацию (с помощью энкодера), так и точные локальные детали (с помощью декодера). Особенностью U-Net является использование «пропускных соединений» (skip connections), которые передают информацию с энкодера напрямую в декодер, что позволяет восстанавливать детали, потерянные в процессе сжатия информации. Это обеспечивает высокую точность сегментации, особенно в задачах, требующих четкого определения границ структур, например, при выделении опухолей или органов на изображениях КТ и МРТ. Широкое распространение U-Net обусловлено её адаптивностью к различным типам изображений и возможностью применения в различных клинических задачах.
nnU-Net представляет собой фреймворк, автоматизирующий процесс проектирования архитектур U-Net для задач сегментации изображений. В отличие от ручной настройки, nnU-Net автоматически определяет оптимальные параметры конфигурации сети, такие как размер патчей, глубину сети, и функции потерь, исходя из характеристик входного набора данных. Это достигается путем анализа статистических данных набора данных, включая размер изображений, разрешение и распределение интенсивностей, для адаптации архитектуры U-Net к конкретной задаче. Автоматизация позволяет значительно сократить время разработки и повысить производительность модели на различных наборах данных, требуя минимального вмешательства эксперта.
Эффективные стратегии мультимодальной фузии, такие как ранняя фузия (Early Fusion), поздняя фузия (Late Fusion) и фузия на основе механизмов внимания (Attention-Based Fusion), играют ключевую роль в интеграции дополнительной информации, получаемой из различных модальностей визуализации. Ранняя фузия объединяет данные из разных модальностей на ранних этапах обработки, позволяя модели сразу учитывать взаимосвязи между ними. Поздняя фузия обрабатывает данные каждой модальности независимо, объединяя результаты на более поздних этапах. Фузия на основе механизмов внимания динамически взвешивает вклад каждой модальности, акцентируя внимание на наиболее релевантных признаках для конкретной задачи. Выбор оптимальной стратегии зависит от характеристик данных и решаемой задачи, поскольку каждая из них имеет свои преимущества и недостатки в плане вычислительной сложности и эффективности.
Традиционные методы сегментации, такие как U-Net и nnU-Net, несмотря на свою эффективность, могут быть вычислительно затратными, особенно при обработке изображений высокого разрешения или больших объемов данных. Кроме того, они часто испытывают трудности при сегментации опухолей сложной формы или с нечеткими границами, что приводит к снижению точности и необходимости ручной коррекции. Для решения этих проблем активно исследуются новые подходы, такие как UNETR, использующие трансформеры для захвата глобального контекста и улучшения сегментации сложных структур, обеспечивая потенциальное повышение эффективности и точности по сравнению с классическими архитектурами.
Фундаментальные модели и возможности MedSAM
Предварительно обученные фундаментальные модели, созданные на основе обширных наборов данных, демонстрируют значительный потенциал в улучшении производительности и надежности сегментации медицинских изображений. Традиционные методы сегментации часто требуют больших объемов размеченных данных для каждой конкретной анатомической структуры и модальности изображения. В отличие от них, фундаментальные модели, используя знания, полученные в процессе обучения на больших неразмеченных данных, способны к обобщению и адаптации к новым задачам с меньшим количеством размеченных данных. Это особенно важно в медицинской визуализации, где получение качественных аннотаций является трудоемким и требует участия квалифицированных специалистов. Использование фундаментальных моделей позволяет снизить зависимость от размеченных данных, повысить точность и устойчивость сегментации, а также упростить процесс разработки и внедрения систем анализа медицинских изображений.
Модель MedSAM является расширением Segment Anything Model (SAM) и адаптирована для применения в медицинской области. В отличие от традиционных методов сегментации, требующих предварительного обучения для каждого конкретного органа или структуры, MedSAM использует подход, основанный на подсказках (prompts). Это позволяет модели выполнять сегментацию различных анатомических объектов, используя в качестве входных данных лишь небольшое количество подсказок, таких как точки или ограничивающие рамки. Такой подход обеспечивает гибкость и адаптивность к различным медицинским изображениям и задачам сегментации, упрощая процесс адаптации к новым анатомическим структурам без необходимости повторного обучения модели с нуля.
Адаптивная разработка запросов (prompt engineering) в MedSAM позволяет оптимизировать процесс сегментации, фокусируясь на релевантных характеристиках подрегионов опухоли. В отличие от универсальных запросов, адаптивные запросы формируются с учетом специфики анатомической области и типа ткани, что повышает точность выделения границ опухоли и ее компонентов. Это достигается путем использования специализированных признаков и контекстной информации, что позволяет модели игнорировать несущественные детали и концентрироваться на ключевых элементах, необходимых для точной сегментации. В результате, адаптивное проектирование запросов способствует улучшению показателей Dice score и других метрик оценки качества сегментации, особенно в сложных случаях, таких как сегментация опухолей головного мозга.
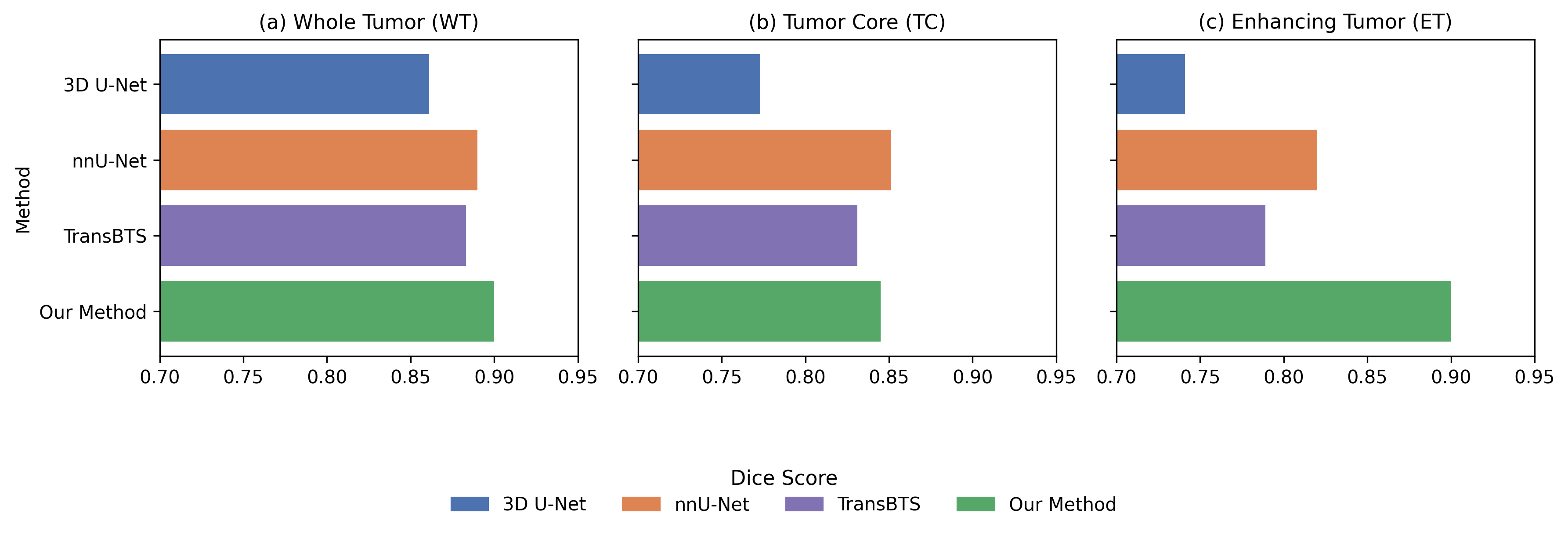
Подход, основанный на предварительном обучении модели на больших объемах данных и последующей целевой промт-инженерии, продемонстрировал высокую эффективность в сегментации опухолей головного мозга. В частности, применение данного метода к набору данных BraTS 2020 позволило достичь среднего значения коэффициента Dice в 0.9012. Это указывает на значительное улучшение точности сегментации по сравнению с традиционными методами, благодаря способности модели адаптироваться к специфическим особенностям анатомических структур и опухолевых образований при помощи правильно сформулированных запросов.
Оптимизация мультимодального слияния с учетом подрегионов
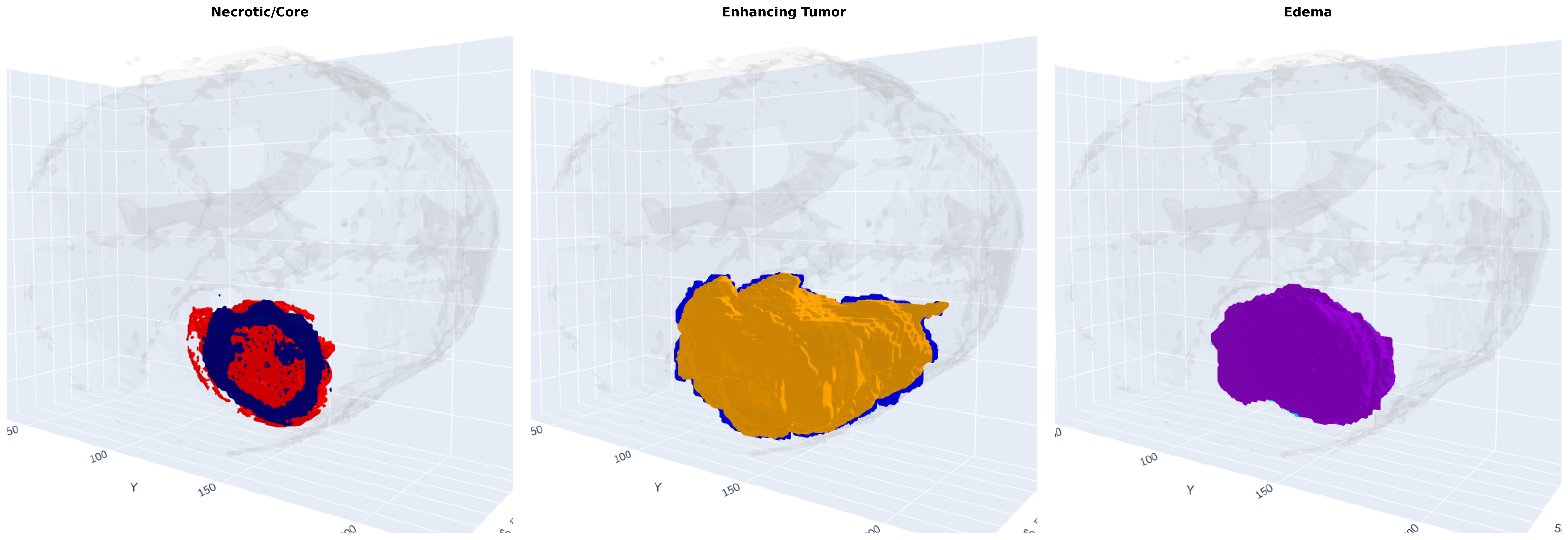
В рамках исследования была разработана система внимания, адаптирующая веса различных модальностей (например, МРТ, КТ) в зависимости от характеристик конкретных подрегионов опухоли. В отличие от традиционных методов, которые применяют единый набор весов ко всей опухоли, данная система анализирует особенности каждого подрегиона — некротического ядра, отечной зоны, контрастирующего узелка и т.д. — и динамически корректирует вклад каждой модальности. Такой подход позволяет более точно выделить границы опухоли, особенно в сложных участках, где одна модальность может быть недостаточно информативной, а другая — более чувствительной к специфическим особенностям конкретного подрегиона. Адаптивное взвешивание модальностей, основанное на анализе подрегионов, значительно повышает точность сегментации опухоли и обеспечивает более надежные результаты диагностики.
В рамках исследования для достижения баланса между высокой производительностью и вычислительной эффективностью был использован TinyViT — облегчённый энкодер на основе архитектуры Transformer. В отличие от более сложных и ресурсоёмких моделей, TinyViT позволяет значительно сократить объём необходимых вычислений без существенной потери точности сегментации опухолей. Этот подход особенно важен при работе с медицинскими изображениями большого размера, где вычислительные затраты могут стать ограничивающим фактором. Применение TinyViT позволяет эффективно обрабатывать данные, обеспечивая возможность использования разработанного метода на широком спектре аппаратных платформ, включая устройства с ограниченными ресурсами, и открывает перспективы для его интеграции в клиническую практику.
Предложенная стратегия целевого объединения модальностей демонстрирует значительное повышение точности сегментации, особенно в областях, традиционно представляющих сложность для анализа, таких как некротический центр опухоли. Результаты исследований показали достижение показателя Dice Score в 0.71 для сегментации некротического центра, что на 10.9% превосходит результаты, полученные с использованием базовых методов. Кроме того, улучшенная сегментация самой опухоли позволила добиться прироста в 9.8% по показателю Dice Score в сравнении с архитектурой nnU-Net, что свидетельствует о высокой эффективности подхода в решении задач точной диагностики и планирования лечения.
Сочетание MedSAM с механизмом внимания, учитывающим особенности подрегионов опухоли, представляет собой существенный прорыв в области надежной и точной сегментации опухолей головного мозга. Данный подход позволяет адаптировать процесс объединения информации из различных модальностей (например, МРТ и КТ) в зависимости от характеристик конкретной области опухоли — её ядра, периферии или зон отека. Это позволяет более эффективно выделять границы опухоли, особенно в сложных случаях, когда традиционные методы сталкиваются с трудностями. Результаты исследований демонстрируют значительное улучшение точности сегментации, что открывает новые возможности для планирования лечения и мониторинга состояния пациентов.
Исследование демонстрирует изящное решение сложной задачи сегментации опухолей мозга, объединяя различные модальности MRI данных и адаптируя подход к специфическим подрегионам опухоли. Такой подход, направленный на повышение точности, особенно в отношении некротического ядра, напоминает о важности гармонии между данными и алгоритмом. Как однажды заметил Ян ЛеКун: «Машинное обучение — это не просто построение моделей, это создание систем, которые понимают мир вокруг нас». Данная работа, фокусируясь на детальном анализе подрегионов и адаптивной обработке данных, воплощает в себе это понимание, демонстрируя, что истинная эффективность достигается через глубокое проникновение в суть проблемы и элегантное решение.
Куда Далее?
Представленная работа, безусловно, демонстрирует элегантность подхода к интеграции мультимодальных данных и адаптивной оптимизации предсказаний. Однако, не стоит обманываться кажущейся завершенностью. Вопрос о действительно глубоком понимании структуры опухоли, а не просто о точном очерчивании границ, остаётся открытым. Авторы сосредоточились на улучшении сегментации, но истинная ценность медицинского изображения заключается в диагностике и прогнозировании — аспектах, требующих не только точности, но и интерпретируемости.
Очевидным направлением для дальнейших исследований является расширение анализа суб-регионов. Необходимо перейти от простого выделения некротического ядра к детальному изучению его микроструктуры и гетерогенности. Использование данных, полученных с помощью других модальностей, таких как ПЭТ или спектроскопия МРТ, могло бы значительно обогатить понимание биологии опухоли. Более того, адаптация фреймворка для работы с данными, полученными от разных пациентов и сканеров, остаётся сложной задачей, требующей разработки устойчивых к вариациям алгоритмов.
В конечном счёте, задача не в том, чтобы создать идеальный алгоритм сегментации, а в том, чтобы построить систему, способную предоставить врачу наиболее полную и достоверную информацию для принятия обоснованных клинических решений. И пусть элегантность не станет самоцелью, а лишь отражением глубины понимания и гармонии между формой и функцией.
Оригинал статьи: https://arxiv.org/pdf/2601.15734.pdf
Связаться с автором: https://www.linkedin.com/in/avetisyan/
Смотрите также:
- Деформация сеток: новый подход на основе нейронных операторов
- Новые смартфоны. Что купить в марте 2026.
- Российский рынок акций: нефть, ставки и дивиденды: что ждет инвесторов в ближайшее время? (05.03.2026 16:32)
- Лучшие смартфоны. Что купить в марте 2026.
- vivo iQOO Z10x ОБЗОР: яркий экран, удобный сенсор отпечатков, объёмный накопитель
- Нефть и бриллианты лидируют: обзор воскресных торгов на «СПБ Бирже» (08.03.2026 16:32)
- Что такое Bazzite и лучше ли она, чем Windows для PC-гейминга? Я установил этот набирающий популярность дистрибутив Linux, чтобы проверить это самостоятельно.
- Infinix Note 60 Ultra ОБЗОР: скоростная зарядка, объёмный накопитель, отличная камера
- Неважно, на что вы фотографируете!
- Ближний Восток и Рубль: Как Геополитика Перекраивает Российский Рынок (02.03.2026 20:32)
2026-01-23 23:36
